Descubren cómo el intestino le indica al cerebro que suprima el hambre durante una infección
Foto: Archivo – Todos los derechos reservados
Un equipo de investigadores ha revelado el mecanismo por el cual los parásitos intestinales activan una señal que viaja desde el sistema inmunitario hasta el cerebro, abriendo nuevas vías potenciales para el tratamiento de enfermedades intestinales o trastornos alimentarios de manera más específica.
El equipo liderado por David Julius, ganador del Premio Nobel de Medicina en 2021 por sus descubrimientos sobre cómo percibimos la temperatura, el dolor y la presión, ha identificado cómo se transmite la señal que suprime el apetito desde el intestino al cerebro en situaciones de infección parasitaria. Este hallazgo es significativo ya que identifica el mecanismo por el cual células sin conexión sináptica directa desencadenan una respuesta que llega al sistema nervioso y altera el comportamiento.
Los autores del estudio, publicado en la revista *Nature*, rastrearon la ruta molecular que conecta el sistema inmunitario intestinal con el cerebro durante una infección por gusanos parásitos. Identificaron un sistema de comunicación inesperado entre dos tipos de células, que resulta en una pérdida de apetito similar a la que se experimenta durante una gastroenteritis. El conocimiento de este mecanismo podría mejorar la comprensión de diversas afecciones que involucran molestias intestinales, desde intolerancias alimentarias hasta el síndrome del intestino irritable.
Un diálogo celular crucial
“La pregunta que queríamos responder no era solo cómo el sistema inmunitario combate a los parásitos, sino cómo recluta al sistema nervioso para modificar el comportamiento”, explica Julius. “Resulta que existe una lógica molecular muy elegante que explica cómo sucede esto”.
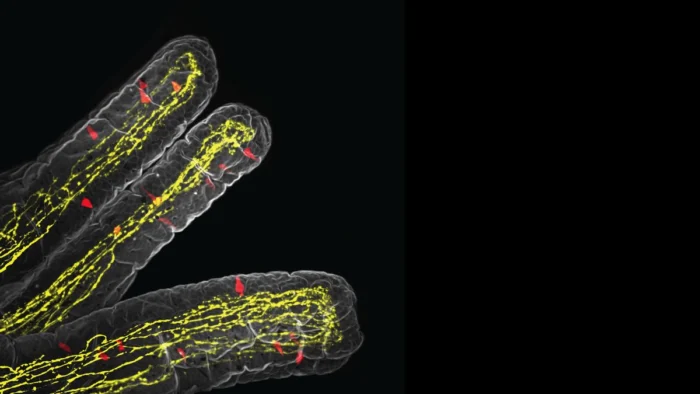
La relación descubierta por el equipo de Julius se establece entre dos tipos de células poco comunes en el intestino: las células en penacho (o células tuft), que detectan parásitos y activan las defensas inmunitarias, y las células enterocromafines (EC), que liberan señales que activan las fibras nerviosas conectadas al cerebro. Se sabía que las primeras provocan sensaciones como náuseas, dolor y malestar intestinal, pero se desconocía si se comunicaban con las células en penacho.
Richard Locksley, inmunólogo de la UCSF y coautor principal, señala: “En mi laboratorio llevamos mucho tiempo interesados en cómo las células en penacho, después de responder inicialmente a una infección parasitaria, liberan señales a otros tipos de células”. Koki Tohara, primera autora del estudio, descubrió que al exponer las células en penacho a moléculas de succinato emitidas por el gusano parásito, estas liberaban acetilcolina, un mensajero químico utilizado principalmente por las neuronas. Posteriormente, al añadir acetilcolina a tejido intestinal cultivado en laboratorio que contenía células EC, estas liberaron serotonina, activando las fibras del nervio vago que transmiten señales del intestino al cerebro.
Esto explica por qué al principio te sientes bien, pero luego empiezas a sentirte mal. El intestino espera a confirmar que la amenaza es real y persistente antes de indicarle al cerebro que cambie tu comportamiento
David Julius, Investigador de la UC San Francisco y líder del estudio
Tohara explica: “Lo que descubrimos es que las células en penacho hacen algo que hacen las neuronas, pero mediante un mecanismo completamente diferente. Utilizan acetilcolina para comunicarse, pero sin la maquinaria celular habitual de la que dependen las neuronas para liberarla”.
El equipo también descubrió que las células en penacho liberan acetilcolina en dos fases distintas: una breve ráfaga en la primera fase y una liberación lenta y sostenida cuando el sistema inmunitario ha generado una respuesta completa. Esto explica por qué las personas a menudo no pierden el apetito hasta varios días después de que comienza la infección.
Julius resume: “Esto explica por qué al principio te sientes bien, pero luego empiezas a sentirte mal a medida que la infección se establece. El intestino básicamente espera a confirmar que la amenaza es real y persistente antes de indicarle al cerebro que cambie tu comportamiento”.
Implicaciones más allá de los parásitos
Los autores comprobaron el mecanismo en experimentos con ratones, infectándolos con un gusano parásito y monitorizando su ingesta de alimentos. Los animales con las células en penacho intactas comieron menos a medida que la infección se extendía. Los ratones modificados genéticamente para carecer de la maquinaria productora de acetilcolina en sus células en penacho siguieron comiendo con normalidad, confirmando que la cadena molecular impulsa la respuesta conductual.
El resultado es relevante para entender mecanismos de defensa en otros epitelios barrera, como las vías respiratorias, expuestas a virus, bacterias y otras infecciones por hongos
Félix Viana, Experto en neurobiología del dolor y la inflamación del Instituto de Neurociencias de Alicante (UMH-CSIC)
Según los autores, estos nuevos hallazgos podrían ser relevantes para el tratamiento de los síntomas de una infección parasitaria. “Controlar la producción de células en penacho podría ser una forma de controlar algunas de las respuestas fisiológicas asociadas con estas infecciones”, sostiene Locksley. El estudio también podría tener implicaciones más amplias, ya que las células en penacho se encuentran en todo el cuerpo, desde las vías respiratorias, la vesícula biliar y el tracto reproductivo. El descubrimiento podría contribuir a conocer mejor afecciones como el síndrome del intestino irritable, las intolerancias alimentarias y el dolor visceral crónico.
El intestino como interfaz sensorial
Félix Viana, experto en neurobiología del dolor y la inflamación del Instituto de Neurociencias de Alicante (UMH-CSIC), considera el artículo interesante y destaca la creatividad del abordaje de David Julius. “Aquí continúa en la senda de entender mecanismos de comunicación paracrina en relación a trastornos gastrointestinales y dolor visceral”, asegura. En su opinión, el resultado también es “relevante para entender mecanismos de defensa en otros epitelios barrera, como las vías respiratorias, expuestas a virus, bacterias y otras infecciones por hongos”.
José Luis Trejo, investigador del Centro de Neurociencias Cajal (CNC-CSIC), considera que este resultado muestra el epitelio intestinal como una interfaz sensorial. “Este trabajo descubre que el epitelio intestinal puede controlar la conducta a través de señales químicas no neuronales y dependientes del tiempo”, asegura. “Esto, a su vez, podría servir para desarrollar dianas terapéuticas ante problemas digestivos, o utilizar este conocimiento en problemas intestinales derivados, no solo de parásitos”.
Podría servir para desarrollar dianas terapéuticas ante problemas digestivos, o utilizar este conocimiento en problemas intestinales derivados, no solo de parásitos
José Luis Trejo, Investigador del Centro de Neurociencias Cajal (CNC-CSIC)
Trejo también considera particularmente interesante que el sistema funcione en dos fases: una primera fase con liberación aguda y transitoria de acetilcolina, y una segunda fase, solo cuando la infección progresa, con una liberación sostenida de acetilcolina, que termina activando el nervio vago y afectando a la pérdida de apetito.
“Es decir, es una señal bifásica donde solo la componente sostenida tiene consecuencias”, resume. “El sistema no responde a la presencia del estímulo, sino a su persistencia. Solo cuando se supera un umbral temporal y espacial, actúa”.
Un trabajo impresionante con nuevas perspectivas
Francesco de Virgilis, investigador del CNC-CSIC especialista en el eje cuerpo-cerebro, califica el trabajo de impresionante y destaca que aporta muchas cosas nuevas e interesantes. “Se sabía que las células tuft producían el neurotransmisor acetilcolina, pero no se conocía toda la vía de señalización que llegaba al cerebro”, explica.
En su opinión, uno de los aspectos más relevantes es que por primera vez se documenta con detalle una ruta específica en la que, en ausencia de vesículas sinápticas y excitabilidad eléctrica, las células pueden modular la señalización sensorial y controlar la conducta. “Una de las cosas importantes es que hacen una observación más fisiológica, como el hecho de que pierdes el hambre”, señala. “Es un comportamiento muy concreto para el que encuentran una explicación molecular, creo que algo tan secuencial no se ha visto en otros órganos”.
Es un comportamiento muy concreto para el que encuentran una explicación molecular, creo que algo tan secuencial no se ha visto en otros órganos
Francesco de Virgilis, Investigador del CNC-CSIC especialista en el eje cuerpo-cerebro
Para el investigador, el hallazgo abre la puerta a plantearse nuevos tratamientos para varios problemas del intestino. “Y no solo a nivel local, sino que también a nivel distal, es decir, más lejos”, dice. “Por ejemplo, puedes modular el nervio vago o elegir otras dianas para mejorar la respuesta del intestino. Ahora mismo damos antiinflamatorios o corticoides, que son muy fuertes y actúan a nivel sistémico, mientras que esto permitiría plantear soluciones más específicas”.